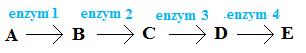Twój wynik: Energia i metabolizm
Analiza
Wszystkie ({{dataStorage.userResults.answersTotal}})
Prawidłowe ({{dataStorage.userResults.answersGood}})
Do powtórki ({{dataStorage.userResults.answersRepeat}})
Błędne ({{dataStorage.userResults.answersBad}})
Pytanie 1
Kilokaloria (kcal) jest
niezbędnym składnikiem pokarmowym
miarą energii, którą komórka wykorzystuje do pracy
miarą energetycznego elektronu
miarą energii cieplnej
miarą temperatury wody
Pytanie 2
Zgodnie z pierwszą zasadą termodynamiki
chaos ustawicznie wzrasta we wszechświecie
energia swobodna jest dostępna do wykonywania pracy w komórce
komórka jest w stanie dynamicznej równowagi
większość pracy w organizmie przypada na pracę mechaniczną
energia może przekształcać się z jednej formy w inną, ale nie może powstawać od nowa i nie ulega zniszczeniu
Pytanie 3
Zgodnie z drugą zasadą termodynamiki
chaos ustawicznie wzrasta we wszechświecie
energia może przekształcać się z jednej formy w inną, ale nie może powstawać od nowa i nie ulega zniszczeniu
energia swobodna jest dostępna do wykonywania pracy w komórce
komórka jest w stanie dynamicznej równowagi
większość pracy w organizmie przypada na pracę mechaniczną
Pytanie 4
W termodynamice ________ jest miarą nieuporządkowania układu.
energia wiązania
praca
entalpia
entropia
katabolizm
Pytanie 5
Reakcję wymagającą dopływu energii swobodnej opisuje się jako
spontaniczną reakcję egzoergiczną
endoergiczną
egzoergiczną
spontaniczną reakcję endoergiczną
spontaniczną
Pytanie 6
Reakcja będzie przebiegać swobodnie, gdy zmiana energii swobodnej (ΔG) będzie miała wartość
zerową
żadną z wymienionych (ΔG nie ma wartości mierzalnej)
dodatnią
dodatnią lub ujemną
ujemną
Pytanie 7
Do tego, by zaszła reakcja wymagająca nakładu energii
energia aktywacji musi wzrosnąć
musi powstawać kompleks enzym-substrat
stężenie ATP musi się zmniejszyć
musi być sprzężona z jakąś reakcją dostarczającą energii
musi być sprzężona z jakąś reakcją wymagającą nakładu energii
Pytanie 8
Która z wymienionych reakcji mogłaby być sprzężona z reakcją endoergiczną
z ΔG = +3,56 kJ/mol?
z ΔG = +3,56 kJ/mol?
reakcja o ΔG równym +6,08 kJ/mol
reakcja o ΔG równym 0 kJ/mol
reakcja o ΔG równym - 1,22 kJ/mol
reakcja o ΔG równym +3,56 kJ/mol
reakcja o ΔG równym -5,91 kJ/mol
Pytanie 9
Rozważ następującą reakcję: glukoza + 602 -> 6C02 + 6H20 (ΔG = -2880 kJ/mol). Które z niżej podanych stwierdzeń dotyczących tej reakcji nie jest prawdziwe?
Reakcja musi być sprzężona z reakcję endoergiczną.
Reakcja jest spontaniczna w znaczeniu termodynamicznym.
Reakcja musi być sprzężona z reakcją egzoergiczną.
Reakcja jest egzoergiczna.
Trzeba dostarczyć nieznaczną ilość energii (energia aktywacji), aby zapoczątkować reakcję, która dalej przebiega z uwolnieniem energii.
Pytanie 10
Energię kinetyczną niezbędną do zapoczątkowania reakcji nazwano
energią swobodną
energią cieplną
energią wiązania
energią aktywacji
energią potencjalną
Pytanie 11
Energia kinetyczna jest
energią stanu
energią wiązań chemicznych
energią zmagazynowaną
energią ruchu
energią położenia
Pytanie 12
Biologicznym katalizatorem, który wpływa na natężenie reakcji chemicznej, nie ulegając przy tym zniszczeniu, jest
enzym
kofaktor
substrat
produkt
koenzym
Pytanie 13
Który z wymienionych inhibitorów wiąże się tylko z miejscem aktywnym enzymu?
inhibitor nieodwracalnie blokujący działanie enzymu
PABA
regulator allosteryczny
inhibitor kompetycyjny
inhibitor niekompetycyjny
Pytanie 14
Na aktywność enzymu może wpływać
PH
temperatura
entalpia
stężenie substratu
kofaktor
Pytanie 15
Który enzym (lub enzymy) z podanej obok sekwencji reakcji prawdopodobnie będzie miał miejsce allosteryczne, z którym może się wiązać końcowy produkt E?
enzym 2
enzym 3
enzym 4
enzym 1
żaden